治験・臨床研究管理センター
治験・臨床研究管理センターの概要
当院では、治験や臨床試験の業務量がここ数年の間に増加した為、2021年4月から治験管理室として独立し、2021年12月からはセンター化に伴い、治験・臨床研究管理センターに名称変更となりました。臨床試験の安全確保や、円滑に臨床試験が実施されることを目的としています。主に治験や臨床研究についての業務を携わっています。
治験・臨床研究とは
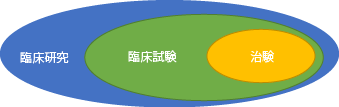
- 臨床研究とは、人を対象に行われるすべての研究を指します。
- 臨床試験は臨床研究の中でも、薬の投与、手術、放射線治療などにより、人体に対して変化を伴う研究です。
- 治験とは、臨床試験の中でも特に、厚生労働省から薬・医療機器としての承認を得ることを目的として行う試験のことです。
治験・臨床研究管理センタースタッフ
医師・薬剤師・事務員・SMO(企業等から委託された治験施設支援機関)で、構成されています。
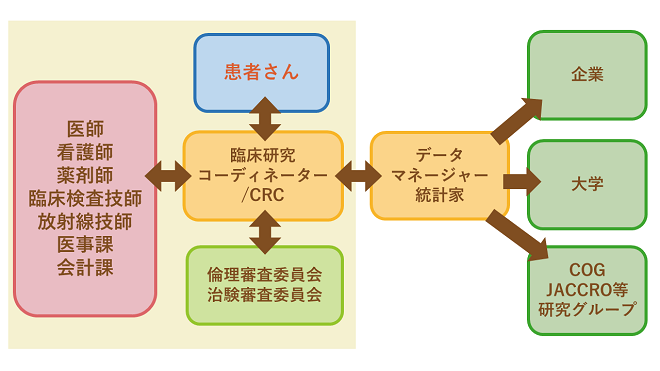
センターの構成メンバー以外、他部署と連携して業務を遂行しています。
治験・臨床研究管理センターの取り組み
企業等から委託された治験施設支援機関の方が治験を医師並びに他職種の方々と連携して行っています。
依頼者さまへ
-
観察研究のお知らせ(研究の公開)
本件は「オプトアウト」すなわち,同意不要であった既存データを用いた研究において,「自分のデータは使わないでほしい」という,患者さんの拒否の機会を確保するため,研究の公開を姫路赤十字病院のホームページ上で一元的に行っているものです。
今回の研究に該当されることが予想され、「自分のデータは使わないでほしい」と希望される方は、ご本人より姫路赤十字病院宛てに手紙、お電話もしくはファックスなどにてその旨ご連絡ください。- 胃がんで通院歴のある患者さんへ
- 「直腸癌術後局所再発のデータベース作成と臨床病理学的研究(多施設共同後向き観察研究)」の実施について
- 高齢者Stage III大腸癌に対する術後補助化学療法の現状調査(多施設共同観察研究)
- 非小細胞肺癌患者における免疫チェックポイント阻害薬治療と臨床的因子の関連性に関する後方視的観察研究
- 非小細胞肺癌患者における免疫チェックポイント阻害薬治療と臨床的因子の関連性に関する後方視的観察研究
- 診断時切除不能 Stage IV 胃癌に対する conversion therapy の治療成績に関する多機関共同観察研究
- HER2陽性切除不能進行・再発胃癌に対するトラスツズマブデルクステカンの有効性・安全性を評価する後ろ向きコホート研究(EN-DEAVOR研究)
- 胃底腺型胃癌におけるリンパ節転移の危険因子に関する多機関共同後ろ向き研究
- 血液・尿・残余腎生検組織を用いたephrin-B2と腎疾患病態への関与の探索
- 未分化型早期胃癌に対する内視鏡的粘膜下層剥離術後の内視鏡的根治度C-2病変における転移・再発危険因子および長期予後に関する検討
- Gastric adenocarcinoma and proximal polyposis of the stomach(GAPPS)に対する実態調査
- 腹腔細胞診陽性の胃がんを対象とした周術期化学療法に関する多施設共同後ろ向き観察研究
- 家族性大腸腺腫症患者レジストリ観察研究
- 血液循環腫瘍DNA陰性の高リスクStageⅡ及び低リスクStageⅢ結腸癌治癒切除例に対する術後補助化学療法としてのCAPOX療法と手術単独を比較するランダム化第Ⅲ相比較試験
患者さんのサポート
採血等の同行や、試験の同意説明の補助を行っています。
医師のサポート
患者さんが適格基準にあっているかどうかのチェックや、プロトコールに沿ったスケジュール管理や臨床データの入力並びに、有害事象発生時の報告の補助も行っています。
薬剤管理
治験薬の温度管理並びに受け入れや払い出しも行っています。
製造販売後調査
厚労省の承認がおりて発売された医薬品の有効性や安全性を確認する調査も行っています。
-
製造販売後調査に使用する書式
-
治験審査委員会 IRB
IRBの資料の作成
当院で実施の治験や臨床研究は、IRB或いは倫理委員会で審査されています。治験審査委員会では「治験実施計画書」が、ヘルシンキ宣言*1に沿って治験に参加される患者さんの人権が守られているか、くすりの効果を科学的に調べられる計画になっているか、治験を行う医師は適切か、参加される患者さんに治験の内容を正しく説明するようになっているかなどを審査します。治験審査委員会には、医療を専門としない者と病院と利害関係がない者が必ず参加します。
ヘルシンキ宣言*1
1964年、世界医師会総会で採択された「ヒトを対象とする生物医学的研究に携わる医師のための勧告」をいう。生物医学的研究は、最終的にヒトを対象とした試験によらなければ、実際の医療に寄与するものにならない。現在の臨床試験は、1964年のヘルシンキ宣言を倫理的基盤としている。このヘルシンキ宣言の重要な原則として、ヒトを対象とする臨床試験を実施するためには、つぎの3項目が必須とされている。
1)科学的・倫理的に適正な配慮を記載した試験実施計画書を作成すること
2)治験審査委員会で試験計画の科学的・倫理的な適正さが承認されること
3)被験者に、事前に説明文書を用いて試験計画について十分に説明し、治験への参加について自由意思による同意を文書に得ること
わが国においては、これらのヘルシンキ宣言の精神に基づいた医薬品の臨床試験の実施に関する基準が、1990年から施行されている。引用元:公益社団法人 日本薬学会
治験審査委員会
IRB委員名簿/こちらからダウンロード
※上記の情報を閲覧するには Adobe Acrobat Readerが必要です。
エキスパートパネル(遺伝子解析結果を検討する委員会)
がん診療連携課とのエキスパートパネルに参加し、企業と連携して推奨された治験を探索し、患者さんの次の治療につなげられるように主治医への情報提供も行っています。
院内各部署との調整
新しい治験や臨床研究が始まるときは、他部署との説明会を開催し、より円滑に進むように調整をしています。
スタッフ紹介
-

中村 進一郎/ なかむら しんいちろう
H5年卒
役職 副院長
- (兼)第一内科部長事務取扱
- (兼)肝胆膵内科部長事務取扱
- (兼)治験・臨床研究管理センター長事務取扱
- (兼)地域医療連携室長事務取扱
- (兼)臨床治療部門長事務取扱
- (兼)DX推進室長事務取扱
- (兼)TQM推進室長事務取扱
専門分野 消化器(肝)
資格 - 日本内科学会総合内科専門医・認定内科医・内科指導医
- 日本消化器病学会認定消化器病専門医・指導医・学会評議員・近畿支部評議員
- 日本肝臓学会認定肝臓専門医・指導医・西部会評議員
- 日本超音波医学会認定超音波専門医・指導医
- 日本消化器内視鏡学会認定消化器内視鏡専門医
- 日本がん治療認定医機構がん治療認定医
- 岡山大学医学部医学科臨床教授
-
上野 聖子/ うえの せいこ
H元卒
役職 薬剤副部長
- (兼)治験・臨床研究管理副センター長
資格 日本薬剤師研修センター 研修認定薬剤師
日本薬剤師研修センター 認定医実務実習指導薬剤師
日本臨床腫瘍学会 がんゲノム医療コーディネーター
肝炎医療コーディネーター
-
地域の先生方へ
より適切な治療を患者さんに提供できるように、地域の先生方と協力して、医療の質の担保と未来の治療に貢献し、地域の方々に還元できるように治験・臨床研究管理センターでサポートしていきたいと思いますので、今後とも宜しくお願いします。





